
2019河南特岗教师招聘考试《理科综合—化学》备考——高频考点
来源:作者: 发布时间:2019-09-02
河南特岗教师招聘考试,理科综合卷题型为单选题、多选题和判断题,总分值100分,其中化学占18分。考查范围为中学化学专业知识。下面就是根据往年考题,对中学化学专业知识进行的分析。具体如下:
考点·离子共存
判断溶液中离子能否大量共存的规律:
多种离子能否大量共存于同一溶液中,归纳起来就是一句话:一色二性四反应。
(1)一色。即溶液颜色。
若题中限定条件为无色溶液,则注意Fe3+、Fe2+、Cr3+、Cr2O72-、CrO42-、MnO4-、Cu2+等有色离子不能存在。
(2)二性。即溶液的酸性和碱性。
在强酸性溶液中,OH-及弱酸根阴离子(如CO32-、SO32-、S2-、CH3COO-等)均不能大量存在;
在强碱性溶液中,H+及弱碱阳离子均不能大量存在;
酸式弱酸根离子在强酸性或强碱性溶液中均不能大量存在。
(3)四反应。
指离子间通常能发生的四种类型的反应,能相互反应的离子显然不能大量共存。
a.复分解反应,如Ba2+与SO42-、NH4+与OH-等;
b.氧化还原反应,如Fe3+与I-,NO3-(+H+)与还原性离子Fe2+等;
c.双水解反应,如Al3+与HCO3-、Al3+与AlO2-、AlO2-与HCO3-等不能大量共存;
d.络合反应,如Fe3+与SCN-等。
考点·离子方程式书写
1.书写离子方程式的注意点:
(1)微溶物处理方式有三种情况
①出现在生成物中写化学式;
②做反应物处于溶液状态写离子符号;
③做反应物处于浊液或固态时写化学式。
(2)浓HCl、浓HNO3在离子方程式中写离子符号,浓H2SO4不写离子符号。
(3)HCO3-、HS-、HSO3-等弱酸盐的酸式酸根离子不能拆开写,强酸盐的酸式酸根离子拆写成离子形式。
(4)注意特殊反应中,各反应物加入的顺序以及加入的量的多少。
例:
AlCl3溶液中滴加NaOH溶液:Al3++3OH-=Al(OH)3↓
NaOH溶液中滴加AlCl3溶液:Al3++4OH-=AlO2-+2H2O
Ca(HCO3)2溶液中加入少量的NaOH溶液:
Ca2++OH-+HCO3-=CaCO3↓+H2O
Ca(HCO3)2溶液中加入过量的NaOH溶液:
Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32-
2.离子方程式正误判断:
(1)观察物质的存在形式和产物是否正确;
(2)看"===="、"
"、"↑"、"↓"(盐类水解产生的沉淀,不写"↓",气体不写"↑",双水解都要写)用的是否恰当;
(3)是否遵守质量守恒和电荷守恒;
(4)是否符合题设条件及要求。如"过量""少量""等物质的量""适量""任意量"以及"滴加顺序"等对反应的影响;
(5)看是否漏掉了某些反应。
考点·阿伏伽德罗常数
1.阿伏加德罗常数的运用是考查和命题的热点。如:已知物质的质量,物质的量,物质的体积,求粒子的数目或比较其粒子的数目大小;已知溶液的体积和浓度,求溶液中溶质的粒子的数目,或比较其粒子的数目大小;已知粒子的数目,求物质的质量,物质的量,物质的体积,溶液中溶质的粒子的浓度或溶液的浓度;物质在发生氧化还原反应时电子转移的数目。
2.解题时要特别注意所给的条件,求什么粒子数,审题要仔细,这种题型教招年年考,但失分者依然较多,主要失误在审题不够仔细。审题时应注意如下细节:
(1)物质的状态:水在标准状况下时为液态或固态;SO3在标准状况下为固态,常温常压下为液态;在标准状况下,碳原子数大于4而小于16的烃为液态,大于等于16的烃为固态。
(2)某些物质的分子中的原子个数,如惰性气体、臭氧(O3)、白磷(P4)等。
(3)一些物质结构中化学键的数目,如SiO2(Si-O四键)、Si、P4(6个P-P键)等。
(4)特别物质的摩尔质量,如D2O,T2O,18O2等。
(5)较复杂的氧化还原反应中,求算转移电子数,如Na2O2+H2O、电解Cu(NO3)2溶液等。
(6)在用到气体摩尔体积22.4L/mol时,必须注意所给物质是否为气体,如果是气体看是否处于标况。
(7)某些离子或原子团水溶液中能发生水解反应,离子数目要改变。
考点·物质的分离、提纯与检验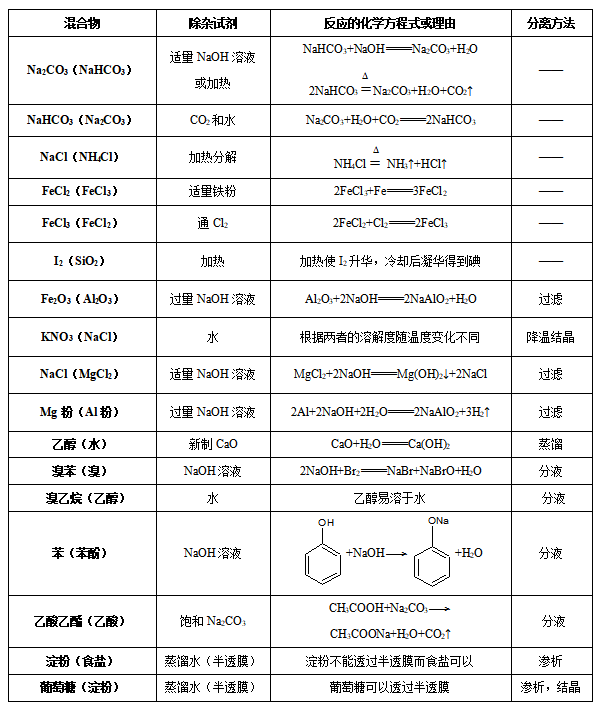
注:本站稿件未经许可不得转载,转载请保留出处及源文件地址。







